ReSCUE微流控平台:培养及释放类器官和类肿瘤,洞察形状对肿瘤生长的影响
2024-12-03 22:51:08 来源:麦姆斯咨询 评论:0 点击:
类器官是一种三维(3D)细胞培养物,可再现人体器官和组织的结构、功能以及细胞复杂性的诸多方面。过去20年来,人类成体干细胞及患者来源性肿瘤样本在类器官中的起动和生长方面取得了重大进展。类器官在很大程度上可以再现患者特异性肿瘤内异质性、基因和蛋白表达、分子特征、代谢活动和组织样微观结构。这种复杂性可能包括基质和脉管成分的结合,在类器官培养期间模拟刺激介导的微环境变化,以及生成不同大小和形状的类器官。值得注意的是,类器官形状对肠道类器官的重要性已经得到证实,通过设计细胞生长成管状有助于类器官培养的寿命。此外,肠道类器官生长产生的隐窝微结构与在体内观察到的相似,隐窝的位置和数量可通过改变干细胞多细胞聚集体的形状来改变。
表面图案化技术已被广泛用于探索类器官形状对二维多细胞聚集体生长和形态的作用。研究发现,人类干细胞聚集体在有图案的基质上的形状,决定了在该基质上生长的神经管样结构的最终形态。狭窄(宽度小于150 µm)的矩形图案会导致U形神经折叠,而较宽的矩形图案则会导致侧向铰链。一项对前列腺癌细胞在图案化表面生长的二维多细胞图案的研究表明,在图案边缘具有正曲率的区域,肿瘤转录因子(例如Oct4和NanoG)的表达量较高。最近的研究表明,长度为数百微米的几何信息,可显著影响细胞迁移、生长动力学以及癌症侵袭。这些研究结果有助于开发出各种形状三维肿瘤球体以及类器官的启动和生长策略,进而提高我们对癌症侵袭的理解。
癌症侵袭是癌症进展的一个主要标志,它们通过不同的肿瘤细胞迁移模式而发生。当细胞间连接减弱时,单个癌细胞可以通过变形或间质运动从肿瘤中分离出来,进入周围组织。另一种情况是,细胞间连接保持不变,肿瘤可通过细胞的集体运动发生侵袭。后一种模式在乳腺癌和肺癌中占主导地位,由肿瘤前缘的突出力驱动,这源于侵袭前线细胞(也称为“领导细胞”)肌动蛋白介导的细胞收缩力。
肿瘤球体和类器官通常在传统的组织培养、生物反应器、旋转瓶、悬滴和微流控平台中生长。然而,形成非球形形态肿瘤球体和类器官的能力仍然存在挑战。最近,有研究采用一种悬滴方法,通过将细胞播种到带有中央支撑微柱的环形三角形、方形或圆形孔中生成非球形类肿瘤。由于微柱周围的细胞压实,培养24小时后,类肿瘤被形成多个片段。此外,这种方法无法提供长期类肿瘤培养所需要的营养物质、氧气的连续流体供应和废物清除。
微流控平台很好的解决了后者的局限性,同时还能生成大小一致的类肿瘤。然而,目前还没有关于形成不同形状类肿瘤以及随后将其从微流控装置中释放以进行下游生物分析(流式细胞术、RNA测序或组织学染色等)的报道。实现对类肿瘤形状的控制并将其从培养环境中靶向释放的能力非常重要,这有助于在三维形态相关的环境中对癌细胞生物学进行深入研究。
据麦姆斯咨询介绍,加拿大多伦多大学的研究人员在Advanced Materials期刊上发表了一篇题为“Microfluidic Platform for Generating and Releasing Patient-Derived Cancer Organoids with Diverse Shapes: Insight into Shape-Dependent Tumor Growth”的论文。该论文报道了一种被称为ReSCUE(Recoverable-Spheroid-on-a-Chip with Unrestricted External Shape)的多层微流控平台,它能生成大小一致、不同形状的类肿瘤和类器官,并能从微流控装置中有选择地释放,用于研究无约束环境中的癌细胞侵袭。与之前报道的用于肿瘤球体和类器官形成的微流控平台不同,ReSCUE微流控平台能以靶向(可寻址)的方式回收,进而对感兴趣的类肿瘤和类器官进行分析。重要的是,研究人员展示了ReSCUE微流控平台在乳腺癌患者来源性类器官(PDO)的生成、选择性释放以及下游分析中的应用。对于类肿瘤和PDO,研究人员展示了ReSCUE微流控平台在研究肿瘤形态对集体侵袭影响方面的实用性。
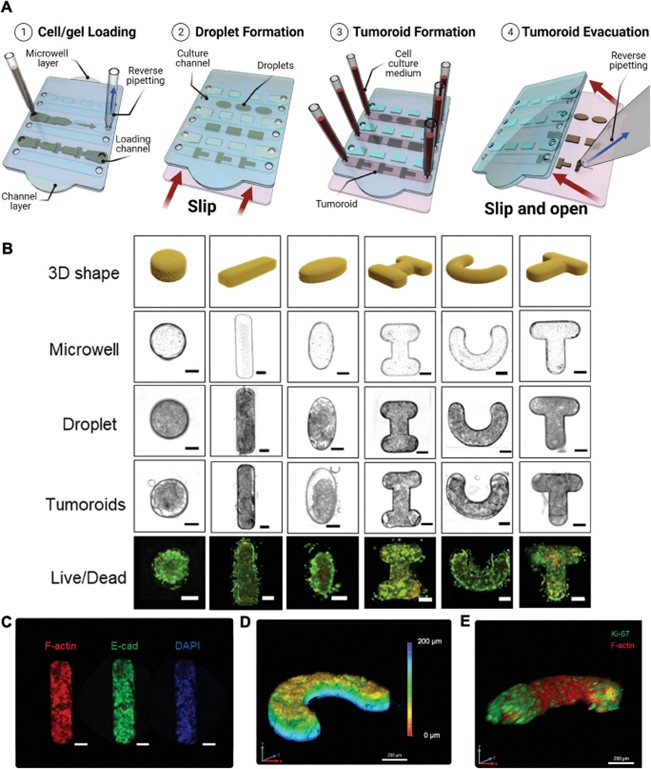
利用ReSCUE微流控平台生成不同形状的类肿瘤
研究人员基于“SlipChip(滑动芯片)”方法开发了一种微流控平台,使用两层疏水改性热塑性塑料层堆叠在一起,允许彼此横向滑动。其中的微孔层包含不同形状的微孔。这些微孔被用于限制装载的细胞,以生成具有所需形状的多细胞类肿瘤或PDO。另一片通道层包含互补的微流控管道和用于细胞培养的微孔。在组装之前,两层都涂上了硅油。硅油是一种密封剂,可防止液体泄漏,同时也是一种润滑剂,有利于两层之间的顺畅滑动。微孔层和通道层组装在一起,将微孔和互补的微流控管道叠加,从而在装置中形成连续的流体通道。
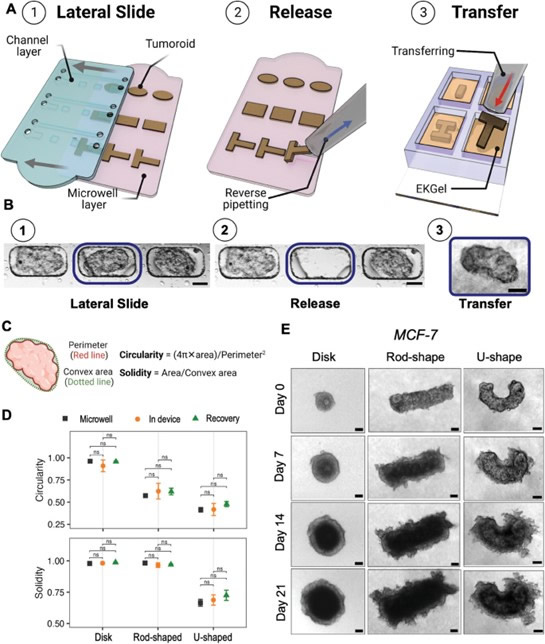
类肿瘤的释放和转移
为了验证ReSCUE微流控平台,研究人员重点研究了由MCF-7乳腺癌细胞组成的类肿瘤。研究人员在微孔层中制作了圆盘形、棒形、椭圆形、U形和I形管道。将ReSCUE微流控平台的两层密封,然后将细胞悬浮液装入由醛功能化纤维素纳米晶体(a-CNCs)和明胶(水凝胶前体)组成的水混合物中,随后横向滑动两层微流控装置,进而在微孔中形成含有细胞的液滴。含有细胞的微凝胶在重力驱动的流体下培养48小时后,高保真、高细胞活性地复制了微孔的形状,产生了盘状、棒状、椭圆形、U形和I形类肿瘤。通过分别对E-cadherin和F-actin进行免疫荧光染色,证实了类肿瘤内细胞-细胞连接的形成和细胞骨架中肌动蛋白的分布。为了验证类肿瘤形态,研究人员培养、回收了U形类肿瘤并对其进行了F-肌动蛋白和Ki-67染色,并使用高分辨率共聚焦显微镜分别观察了细胞骨架丝和增殖性致瘤细胞。无论是在微流控装置中还是释放后,类肿瘤都具有所需要的三维形状,厚度约为200 µm,接近宿主微孔的深度。三维重建以及其他成像结果证明,装载的细胞均匀地分布在类肿瘤内,并充分填充了微孔,从而高保真地生成了所需要的形状。
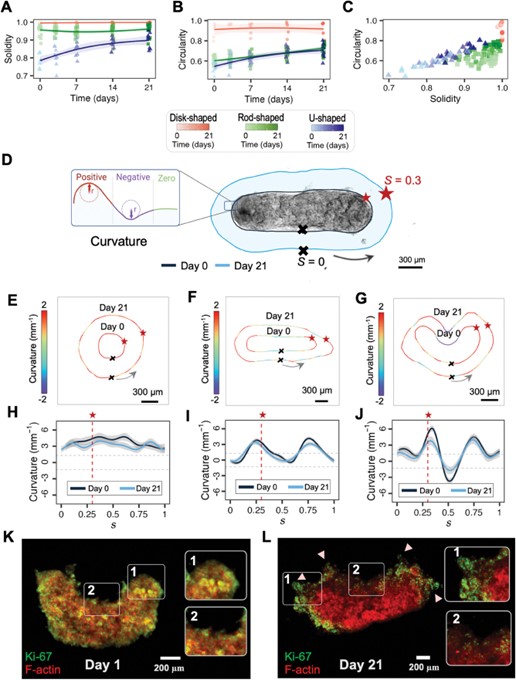
几何形状对类肿瘤的影响
总结来说,ReSCUE微流控平台能够高效地形成不同形态、大小一致的类肿瘤和PDO,随后将其从微流控装置中高保真地释放,并在由三维仿生水凝胶组成的无约束环境中进行恢复后的长期培养。这种能力通过非恶性MCF-10A乳腺上皮细胞和恶性MCF-7乳腺癌细胞系以及两个独立的PDO乳腺癌模型(DCXBTO.58和BPTO.95)都得到了证明,显示了该平台的稳健性和多功能性。重要的是,仅在2天和4天内,就分别形成了数百微米大小的类肿瘤和PDO。类肿瘤和PDO可以一次性从ReSCUE微流控平台中释放,也可通过靶向识别释放,因此释放后能够进行培养和分析,以检查肿瘤的生长情况。在目前的工作中,研究人员探讨了肿瘤形状对细胞集体侵袭的影响,但ReSCUE微流控平台的用途自然可以扩展到研究其它摄动的影响,例如药物治疗或细胞共培养在可控体外环境中对宏观肿瘤结构的影响。
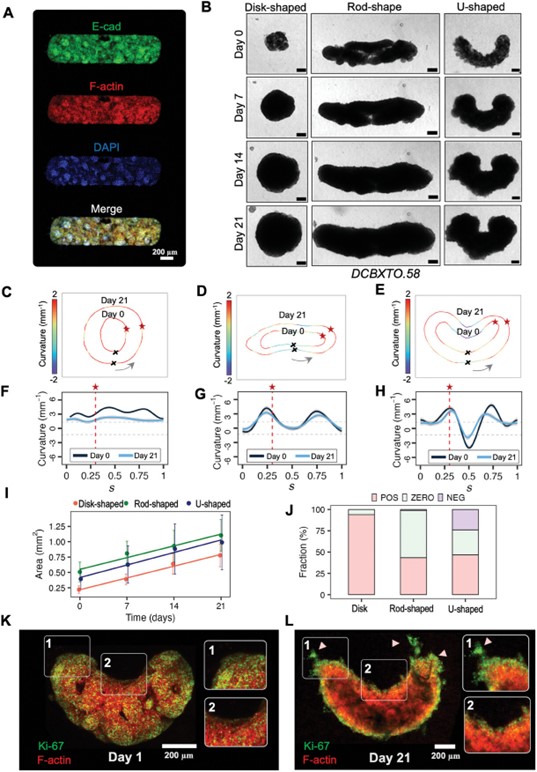
不同形状的乳腺癌患者来源性类器官(PDO)的生成、释放和后期培养
研究人员利用ReSCUE微流控平台探索了类器官形态对其在无约束仿生水凝胶中生长的影响。结果表明,增殖性癌细胞倾向于在正曲率高的类器官部位定位,从而导致其快速生长,而具有不同形状的类器官整体生长模式则倾向于降低类器官-水凝胶界面的界面张力。除了形成形态各异的类器官外,该平台还可以整合到多组织微生理系统中。
此外,ReSCUE微流控平台的应用可以扩展到癌症研究之外,例如用于形成三维肌肉组织作为微型机器人的生物导管,工程化的人体皮质、前脑和膀胱类组装体,以及类器官组织工程。此外,不同形状的人体类组装体或类器官工程还可用于多组织微生理系统(MPS)以及关联的“器官芯片”平台,用于药物筛选或疾病的发展研究。在癌症研究中,肿瘤形态对放射治疗的影响,也是优化放射剂量和选择适当肿瘤切缘的关键研究领域。
论文链接:https://doi.org/10.1002/adma.202410547
延伸阅读:
上一篇:石墨烯生物传感器实现趋化因子的超灵敏检测,为先进诊断技术铺平道路
下一篇:最后一页
